优于伊布替尼!百济神州公布百悦泽临床试验进展
10月12日,泽布替尼发布公告称自主研发产品BTK抑制剂百悦泽®(泽布替尼胶囊)在全球3期ALPINE试验的一项终期分析中,经独立评审委员会(IRC)及研究者评估,百悦泽®对比亿珂®(伊布替尼),取得无进展生存期(PFS)的优效性结果。
ALPINE研究是一项随机、全球3期临床试验(NCT03734016),旨在评估百悦泽®对比亿珂®(伊布替尼),用于治疗既往经治的复发或难治性(R/R)慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者的效果。
据悉,伊布替尼为肿瘤患者常见用药,适用于套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞淋巴瘤等疾病的治疗。资料显示,伊布替尼用药后副作用较多,其中较为严重的副作用主要有:出血、感染、全血细胞减少和肌酐水平增加,而套细胞淋巴瘤患者用药后有可能会导致皮肤癌。
而泽布替尼为百济神州自主研发的潜在同类最优的第二代BTK小分子抑制剂,具有已获证实的临床疗效和安全性,是首款获美国 FDA 批准和突破性疗法认定的中国自主研发的抗癌药。 根据弗若斯特沙利文的报告,在全球范围内,BTK抑制剂在2025年全球市场规模将达到200亿美元;中国BTK抑制剂市场规模预计将于2025年增长至131亿元人民币。
本次泽布替尼胶囊临床试验的成功,使泽布替尼成为全球首个且唯一在CLL、SLL中,“头对头”对比伊布替尼,在PFS方面达到优效性的BTK抑制剂。PFS是CLL治疗中的重要指标之一,在评估患者长期治疗的疗效和生活质量方面具有参考意义。此次ALPINE研究在PFS终期分析中取得积极结果,也再次印证了泽布替尼作为“同类最优”药物的治疗潜力。
据百济神州2022年半年报显示,目前百悦泽®(泽布替尼胶囊)已获得附条件批准用于治疗既往接受过至少一种治疗的MCL成人患者和既往接受过至少一种治疗的CLL或SLL成人患者,以及用于治疗R/R WM患者。此外,NMPA已受理一项百悦泽®用于治疗CLL或SLL初治成人患者的sNDA。
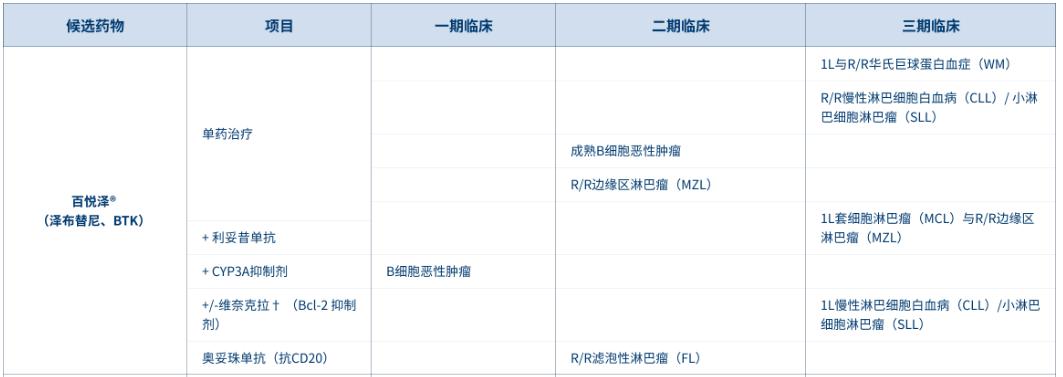
来源:百济神州官网
作为首款出海的本土原研新药,百悦泽®(泽布替尼胶囊)至今已在全球超过50个市场获批,包括美国、中国、欧盟、英国、加拿大、澳大利亚等。在美国,百悦泽®已有三项适应症获批上市;国内方面,百悦泽®获批的三项适应症已全部进入国家医保目录。此外,美国FDA、欧洲药品管理局、加拿大卫生部等多国药品管理机构也已分别受理百悦泽®不同适应症的上市申请。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管92.42
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.26
- 监管中axi15-20年 | 澳大利亚监管 | 英国监管 | 新西兰监管79.20
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中Moneta Markets亿汇澳大利亚| 2-5年| 零售外汇牌照82.07
- 监管中GTCFX10-15年 | 阿联酋监管 | 毛里求斯监管 | 瓦努阿图监管60.90
- 监管中VSTAR塞浦路斯监管| 直通牌照(STP)80.00
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.81
- 监管中金点国际集团 GD International Group澳大利亚| 1-2年86.64
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56


