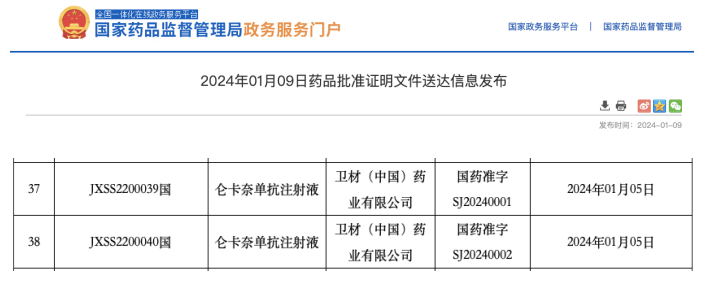
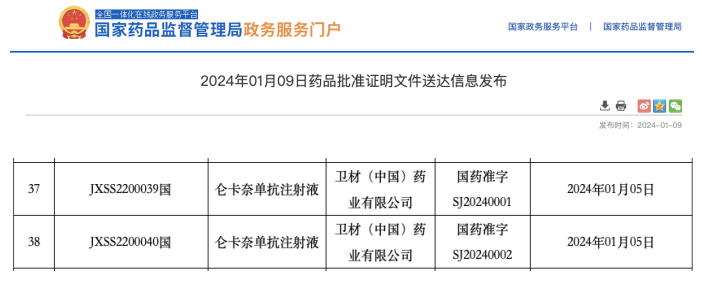
卫材仑卡奈单抗国内获批上市,用于治疗早期阿尔茨海默病
1月9日,据国家药监局披露,卫材(中国)药业有限公司申请的仑卡奈单抗注射液获批上市,受理号为 JXSS2200039/40,用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆。
阿尔茨海默病(AD)是一种起病隐匿的进行性发展的神经退行性疾病,临床特征包括记忆障碍、失语失认等。资料显示,截至2018年,中国60岁以上的人口中,阿尔茨海默病患者有983万人,轻度认知障碍患者有3877万人。据估计,到2050年,阿尔茨海默病患者人数将增至4000万人。
据卫材中国官方微信公号,仑卡奈单抗即人源化抗可溶性β淀粉样蛋白(Aβ)单克隆抗体LEQEMBI®(中文商品名:乐意保®)。仑卡奈单抗既可选择性地与可溶性Aβ聚合物(原纤维)结合,也可以与Aβ斑块的主要成分不溶性的Aβ聚合物(纤维)结合,从而清除大脑中的Aβ原纤维和Aβ斑块。
卫材表示,仑卡奈单抗在中国获批,是基于包括中国在内的全球大型III期研究Clarity AD1。在Clarity AD研究中,仑卡奈单抗达到了主要终点和所有关键次要终点,且结果具有统计学意义。
据了解,与安慰剂相比,LEQEMBI治疗在18个月时减少了CDR-SB的临床下降27%。此外,由AD看护者评估的次要终点阿尔茨海默症协作研究组-轻度认知障碍-日常生活能力量表评分(ADCSMCI-ADL)显示出37%的显著统计学获益。上述内容权衡的是患者独立运作的能力,包括穿衣、喂食、参与社区活动等。
卫材的仑卡奈单抗在中国获批前,还曾于2023年7月在美国获得完全批准、9月在日本获得批准,本次获批也是该产品在第三个国家获批上市。
仑卡奈单抗售价虽暂未公布,不过,2023年10月,仑卡奈单抗通过海南省药品监督管理局审核,落地海南博鳌乐城国际医疗旅游先行区时的定价为3328.2元/瓶。同时据了解,该产品为静脉输注给药,每2周注射一次。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管92.42
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管85.36
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中金点国际集团 GD International Group澳大利亚| 1-2年86.64
- 监管中Moneta Markets亿汇澳大利亚| 2-5年| 零售外汇牌照80.52
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.81
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56
- 监管中GO Markets高汇15-20年 | 澳大利亚监管 | 塞浦路斯监管 | 塞舌尔监管87.90
- 监管中alpari艾福瑞5-10年 | 白俄罗斯监管 | 零售外汇牌照87.05
- 监管中易信easyMarkets15-20年 |澳大利亚监管 | 塞浦路斯监管86.33