业绩亏损、无控股股东,善康医药能否成功科创板IPO?
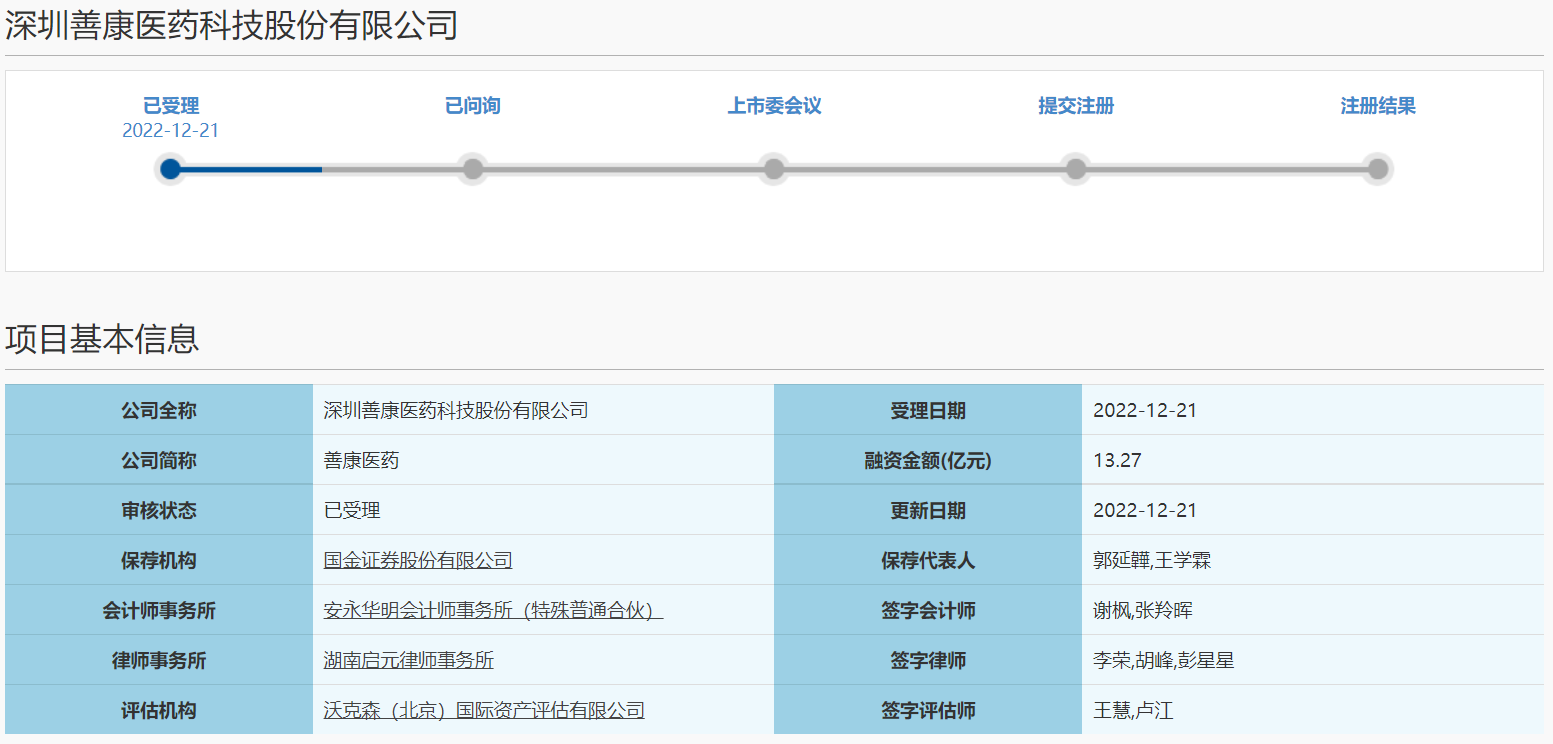
2022年12月21日,深圳善康医药科技股份有限公司(下称“善康医药”)冲刺科创板IPO获上交所受理,本次拟募资13.27亿元。
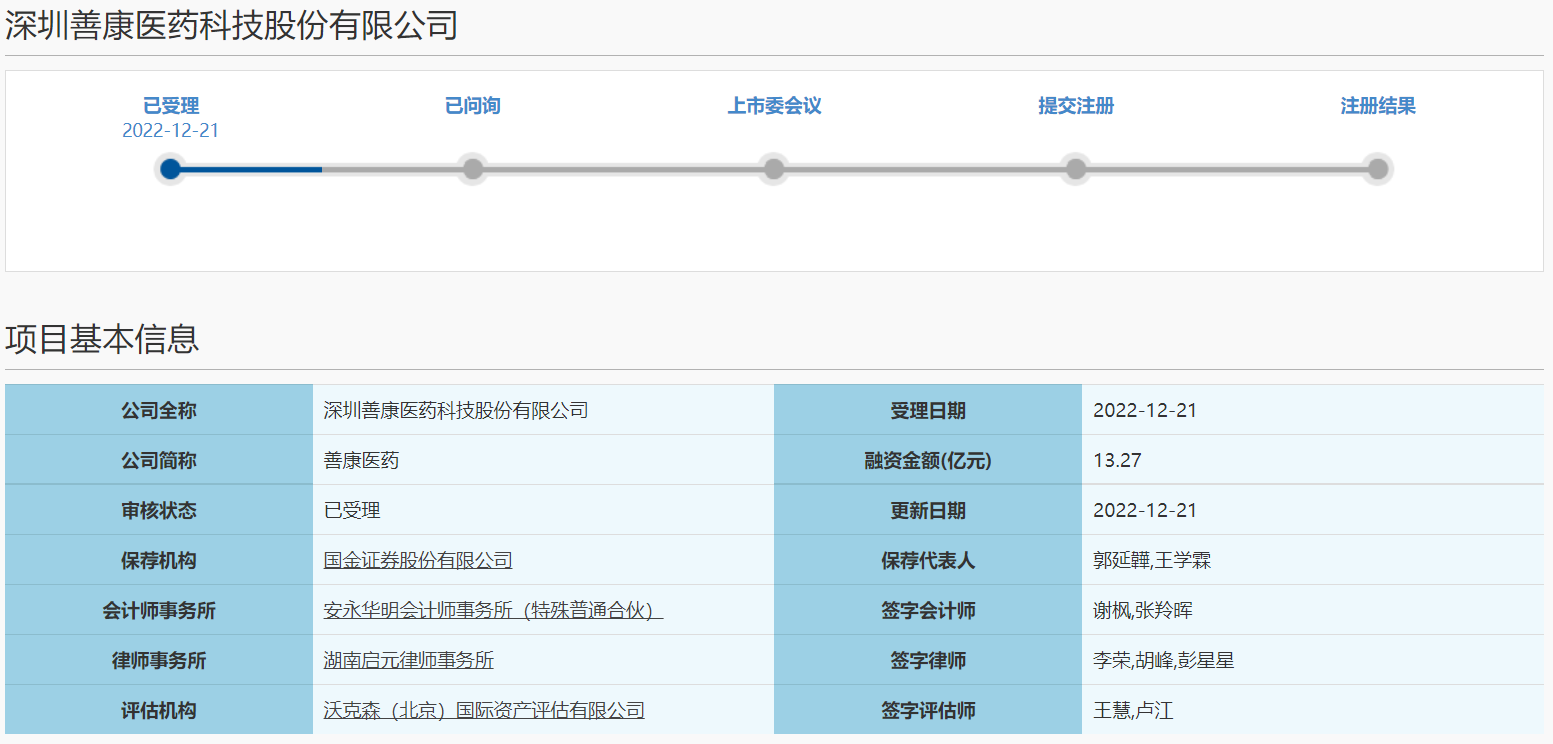
图片来源:上交所官网
善康医药公司主要从事以预防阿片类毒品复吸、治疗酒精使用障碍为代表的成瘾治疗药物等创新药的研发、生产和销售,是一家拥有自主知识产权和全球视野的国际化创新药研发企业,致力于打造成瘾治疗的“中国方案”。
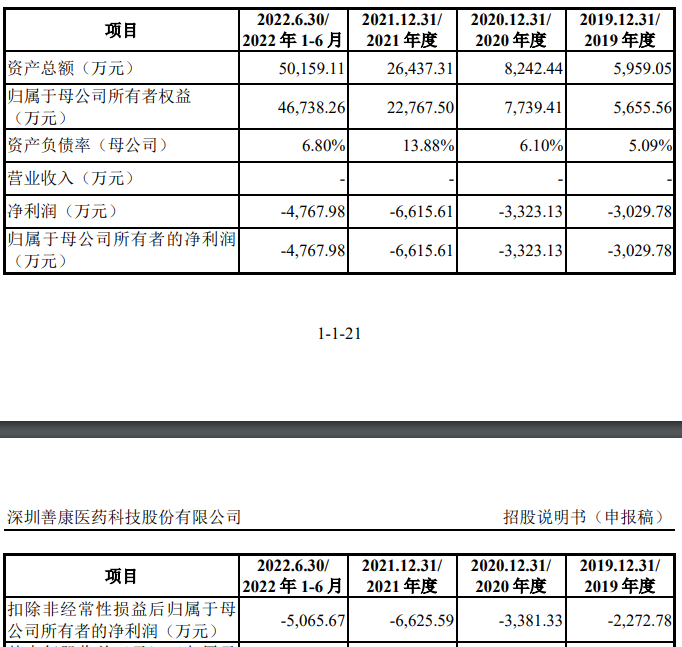
图片来源:公司招股书
财务数据显示,公司2019年、2020年、2021年、2022年前6月归母净亏损分别为3029.78万元、3323.13万元、6615.61万元、4767.98万元。
公司选择《上海证券交易所科创板股票发行上市审核规则》第二十二条之“(五)预计市值不低于人民币40亿元,主要业务或产品需经国家有关部门批准,市场空间大,目前已取得阶段性成果。医药行业企业需至少有一项核心产品获准开展二期临床试验,其他符合科创板定位的企业需具备明显的技术优势并满足相应条件”作为上市标准。发行人核心产品纳曲酮植入剂的2个适应症分别处于产品注册申请准备阶段和Ⅱ期临床阶段,且该产品符合市场空间大的特征。
本次拟募资用于新药研发项目、创新药高端制剂生产基地建设项目、营销网络建设项目、补充流动资金项目。
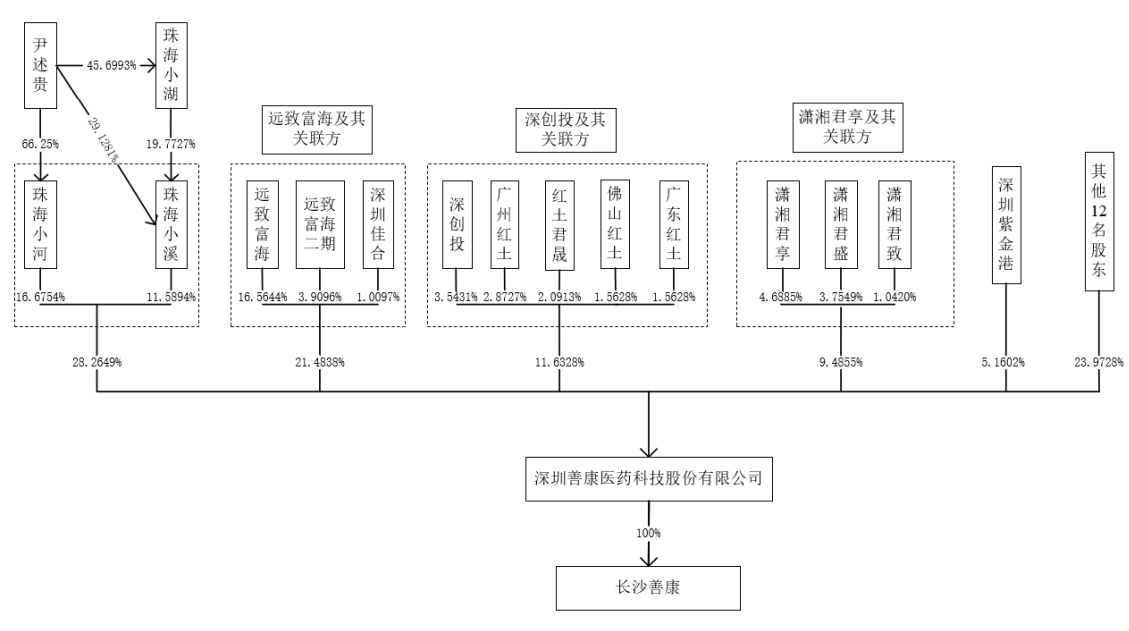
图片来源:公司招股书
善康医药表示,公司无控股股东,公司的实际控制人是尹述贵。尹述贵分别直接持有珠海小河、珠海小溪和珠海小湖66.25%、29.1281%和45.6993%的合伙份额,担任珠海小河、珠海小溪、珠海小湖三家合伙企业执行事务合伙人并实际控制,尹述贵通过三家合伙企业合计控制发行人28.2649%的股份表决权,为公司实际控制人。
善康医药坦言公司面临以下风险:
一、公司是一家拟采用第五套上市标准的生物医药行业公司
公司主要从事以预防阿片类毒品复吸、治疗酒精使用障碍为代表的成瘾治疗药物等创新药的研发、生产和销售,是一家拥有自主知识产权和全球视野的国际化创新药研发企业,致力于打造成瘾治疗的“中国方案”。SK1801(“纳曲酮植入剂”—用于预防阿片类物质成瘾患者脱毒后的复吸)是公司的核心研发产品,该产品经CDE审核同意,将其纳入“突破性治疗品种”名单,公司拟于2022年12月向CDE提交药品上市注册申请。SK2007(“纳曲酮植入剂”—用于治疗酒精使用障碍适应症)已于2022年8月获得Ⅱ期临床试验批准通知书,已在中国启动Ⅱ期临床试验工作。依托于公司以长效缓控释植入剂技术为核心的药物递送系统创新研发平台,多个临床前研究阶段的在研项目也在有序推进中,公司的主要产品符合“市场空间大”的特征,具体详见本招股说明书“第二节概览”之“发行人选择的具体上市标准”。
公司作为一家拟适用《上海证券交易所科创板股票发行上市审核规则》第五套上市标准的生物医药行业公司,目前尚未实现盈利,公司提示投资者关注公司以下特点及风险:
(一)发行人核心产品尚未上市销售,公司尚未盈利并预期持续亏损
公司的核心产品SK1801(“纳曲酮植入剂”—用于预防阿片类物质成瘾患者脱毒后的复吸)拟于2022年12月向CDE提交药品上市注册申请,尚未开展商业化生产销售,发行人尚未盈利且存在累计未弥补亏损。报告期内,发行人归属于母公司所有者的净利润分别为-3,029.78万元、-3,323.13万元、-6,615.61万元和-4,767.98万元。未来一段时间内,公司预期将持续亏损并存在累计未弥补亏损。
(二)发行人上市后可能面临退市的风险
公司若自上市之日起第4个完整会计年度触发《上海证券交易所科创板股票上市规则》第12.4.2条的财务状况,即经审计扣除非经常性损益前后的净利润(含被追溯重述)为负且营业收入(含被追溯重述)低于1亿元,或经审计的净资产(含被追溯重述)为负,则可能导致公司触发退市条件。虽然,公司预计未来4个完整的会计年度内触发该条件的可能性较小;但截至本招股说明书签署日,公司的核心产品尚未取得药品注册证书,未开展商业化生产、销售业务,存在持续无法盈利的可能性,发行人未盈利状态可能持续存在或累计未弥补亏损继续扩大,进而可能导致触发退市条件。根据《科创板上市公司持续监管办法(试行)》,公司触及终止上市标准的,股票直接终止上市,不再适用暂停上市、恢复上市、重新上市程序。
三、新药研发及商业化相关的风险
(一)SK1801审批进度不及预期的风险
发行人拟于2022年12月向CDE提交SK1801(“纳曲酮植入剂”—用于预防阿片类物质成瘾患者脱毒后的复吸)的药品上市注册申请,预计该品种于2023年可获得上市批准。但由于药品研发及注册审评审批环节较多、周期较长、不确定性较大,如发行人SK1801的新药注册上市审评审批进程受到较大程度的延迟或无法获得上市批准,则将对公司未来的业务及经营业绩造成较大不利影响。
(二)发行人在研产品临床试验结果不及预期的风险
发行人SK2007(“纳曲酮植入剂”—用于治疗酒精使用障碍)已获得CDE同意豁免I期临床试验,直接进入Ⅱ期临床试验,此外发行人还有多款在研产品预计于2023年后陆续进入临床试验。由于创新药的研发具有高投入、长周期及高风险的特点,发行人无法保证任何临床前研究以及早期临床研究数据能够预测候选药物的临床结果。若发行人的临床试验数据结果不能达到预期,发行人将可能放弃临床试验的后续研发工作,将使得发行人对该产品的前期研发投入无法收回,发行人未来的盈利能力也将受到重大不利影响。
(三)单一产品依赖风险
发行人的核心产品为纳曲酮植入剂,该产品用于预防阿片类物质成瘾患者脱毒后的复吸适应症,拟于2022年12月向CDE提交药品上市注册申请,并拟在美国开展临床试验;用于治疗酒精使用障碍适应症已获批Ⅱ期临床,但相关临床试验尚在开展过程中;发行人的其他在研产品尚处于临床前研究阶段。因此,在一段时期内,发行人将依赖于纳曲酮植入剂产品获批上市后的商业拓展,公司的盈利能力受到单一产品的限制。若纳曲酮植入剂的商业化进展达不到预期,将对公司盈利能力带来不利影响。
(四)产品商业化风险
1、若销售团队招募及发展达不到预期,将影响公司未来的商业化能力
鉴于纳曲酮植入剂预计在2023年正式获批,发行人已着手组建相应销售团队,并计划采用以直销为主、经销为辅的自主销售模式,同时积极推动该品种进入政府采购。公司拟利用本次公开发行募集资金在南京、广州、武汉、北京、西安、成都、沈阳共建立7个区域级营销办事处,形成覆盖全国华东、华南、华中、华北、西北、西南、东北等多个地区的营销网络布局。此外,公司将扩充营销团队,组建国际化专业营销队伍,根据不同区域患者的文化背景及生活习惯制定特色化营销战略,并积极举办学术推广、业务培训等营销活动,积极推动核心产品纳曲酮植入剂在国外的临床试验,为公司后续新药在国内及国际上市奠定充分市场基础。随着发行人纳曲酮植入剂新药注册上市获批和市场化拓展的推进,目前的营销策略可能无法完全符合未来市场实际情况,也可能在市场推广过程中面临缺乏专业市场人员或营销推广经验不足的困难,或存在市场营销人才流失的风险,这将对公司的商业化能力造成不利影响,从而对公司的业务、财务状况及经营业绩造成不利影响。
2、纳曲酮植入剂的商业化推广不及预期风险
发行人的SK1801(“纳曲酮植入剂”—用于预防阿片类物质成瘾患者脱毒后的复吸)相较于已上市竞品在疗效、患者依从性及安全性等方面具有明确优势。但是,纳曲酮植入剂的商业化推广需要经过监管机构沟通、学术推广和市场拓展等较长的市场教育阶段,同时其销售的快速增长可能会依赖戒毒医疗机构的覆盖面。如在市场拓展、学术推广、戒毒医疗机构覆盖等方面的进展未达预期,未能有效获得医生和患者的认可或未能实现快速销售放量,则可能影响公司收入增长及盈利能力的提升。
四、实际控制人持股比例较低风险
截至本招股说明书签署日,尹述贵通过控制珠海小河、珠海小溪、珠海小湖,可以间接控制公司28.2649%表决权,为公司实际控制人。
按照本次发行上限测算,本次发行后尹述贵合计控制公司表决权比例将降至21.1987%。由于实际控制人持股比例较低,上市后潜在投资者通过股权收购或其他原因,可能使得实际控制人控制地位不稳定,将对公司未来的经营发展带来不利影响。
(来源:界面AI)
声明:本条内容由界面AI生成并授权使用,内容仅供参考,不构成投资建议。AI技术战略支持为有连云。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管92.42
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.26
- 监管中axi15-20年 | 澳大利亚监管 | 英国监管 | 新西兰监管79.20
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中Moneta Markets亿汇澳大利亚| 2-5年| 零售外汇牌照82.07
- 监管中GTCFX10-15年 | 阿联酋监管 | 毛里求斯监管 | 瓦努阿图监管60.90
- 监管中VSTAR塞浦路斯监管| 直通牌照(STP)80.00
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.81
- 监管中金点国际集团 GD International Group澳大利亚| 1-2年86.64
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56